Sarepta (SRPT)...Achtung HOCHSPEKULATIV: USD 19.44 am 8.6.2016 (Totalverlust oder Tenbagger?) - 500 Beiträge pro Seite
eröffnet am 08.06.16 22:57:18 von
neuester Beitrag 25.01.21 18:23:41 von
neuester Beitrag 25.01.21 18:23:41 von
Beiträge: 57
ID: 1.233.251
ID: 1.233.251
Aufrufe heute: 0
Gesamt: 9.011
Gesamt: 9.011
Aktive User: 0
ISIN: US8036071004 · WKN: A1J1BH · Symbol: AB3A
106,30
EUR
-6,67 %
-7,60 EUR
Letzter Kurs 16:13:28 Tradegate
Neuigkeiten
| Titel |
|---|
03.05.24 · Business Wire (engl.) |
01.05.24 · Business Wire (engl.) |
01.05.24 · Business Wire (engl.) |
24.04.24 · Business Wire (engl.) |
29.03.24 · Business Wire (engl.) |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,0450 | +14.021,62 | |
| 42,00 | +105,88 | |
| 1,7870 | +28,56 | |
| 37,00 | +26,71 | |
| 36,85 | +21,18 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 7,8165 | -26,67 | |
| 1,7000 | -31,17 | |
| 2,3450 | -47,60 | |
| 0,5008 | -50,90 | |
| 3,5300 | -55,71 |
ACHTUNG: HOCHSPEKULATIV!
Duchenne, kurz DMD, ist eine X-chromosomal-rezessiv vererbte Muskelerkrankung, die sich in der frühen Kindheit manifestiert und rasch zu Muskelschwäche, Atrophie der Muskulatur und Rollstuhlpflicht führt. Da die Krankheit X-chromosomal-rezessiv vererbt wird, sind fast ausschliesslich männliche Nachkommen davon betroffen. Die Erkrankung betrifft einen von 3500 männlichen Neugeborenen und manifestiert sich zwischen dem ersten und dem sechsten Lebensjahr.
Die Erkrankung beginnt im Beckengürtelbereich. Die betroffenen Patienten haben Probleme beim Gehen. Sie sind unsicher und stolpern häufig. Schnelles Laufen ist nicht möglich. Aufgrund der Schwäche der Oberschenkelmuskulatur können sich die Patienten kaum noch alleine aufrichten. Aus diesem Grund stützen sie sich beim Aufrichten mit den Händen am Oberschenkel ab, was auch als Gowers-Zeichen bezeichnet wird. Da die Muskeldystrophie Typ Duchenne vor allem im Bereich der Waden zu einer Zunahme des Fettgewebes und des Bindegewebes führt, erscheinen diese sehr kräftig. Man spricht auch von Gnomenwaden. Zusätzlich werden häufig eine ausgeprägte Lendenlordose und Spitzfüße beobachtet. Die Erkrankung zeigt einen rasch progredienten Verlauf. Im Laufe der Zeit führt die Erkrankung auch zu einer Muskelschwäche und Muskelatrophie an der oberen Extremität mit Scapula alata. Die meisten Patienten sitzen zum Zeitpunkt des 12. Lebensjahres im Rollstuhl. Die Rollstuhlabhängigkeit führt zu einer progredienten Skoliose mit Reduktion der Vitalkapazität. Zusätzlich schränkt eine Schwäche der Atemmuskulatur die Atmung weiter ein.
Wenn die Patienten das zehnte Lebensjahr überschritten haben, wird die zuvor präklinische Kardiomyopathie klinisch relevant. Jeder dritte Patient weist eine Intelligenzminderung auf.
In einem fortgeschrittenen Stadium kommt es zu einer Areflexie. Faszikulationen, Fibrillationen und Sensibilitätsstörungen werden nicht beobachtet. Die Lebenserwartung beträgt ca. 40 Jahre,wobei aber auch vile Patienten bereits im Kindesalter versterben.
Eteplirsen wurde von Sarepta Therapeutics zur Behandlung von Duchenne in der Klinik getestet und befindet sich derzeit im Zulassungsprozedere der amerikanischen Arzneimittelbehörde (FDA). Eine von der FDA einberufene Expertenrunde hat mit 7:6 gegen eine Zulassung gestimmt. Der Zulassungsantrag beruht auf sehr schwachen klinischen Daten, so dass die FDA von 13 Patienten eine Biopsie zum Nachweis von Dystrophin in den Muskelpartien als Folge der Behandlung mit Eteplirsen eingefordert hat.
Unter normalen Umständen hätte dieser Zulassungsantrag keine Chance auf einen positiven Bescheid. In Anbetracht der nicht vorhandenen Therapiemöglichkeiten und dem grausamen Krankheitsverlauf, ist - positive Biopsieergebnisse vorausgesetzt- die Zulassung im Sommer 2016 dennoch nicht ausgeschlossen. Bei ungünstigen Bipsieergebnissen (kein Nachweis von Dystrophin) erfolgt ein Absturz sehr wahrscheinlich unter 5$.
Ich habe mir Heute eine kleine Position zu USD 18.88 ins Depot gelegt und habe diese sofort abgeschrieben!
ACHTUNG: HOCHSPEKULATIV!
Deswegen nur bedingt zur Nachahmung empfohlen! Höchstens Reserven investieren, die SOFORT abgeschrieben werden können. TOTALVERLUST möglich.
Sollte Eteplirsen allerdings zugelassen werden, dann sind dreistellige Kurse aufgrund des Alleinstellungsmerkmales wahrscheinlich.
Duchenne, kurz DMD, ist eine X-chromosomal-rezessiv vererbte Muskelerkrankung, die sich in der frühen Kindheit manifestiert und rasch zu Muskelschwäche, Atrophie der Muskulatur und Rollstuhlpflicht führt. Da die Krankheit X-chromosomal-rezessiv vererbt wird, sind fast ausschliesslich männliche Nachkommen davon betroffen. Die Erkrankung betrifft einen von 3500 männlichen Neugeborenen und manifestiert sich zwischen dem ersten und dem sechsten Lebensjahr.
Die Erkrankung beginnt im Beckengürtelbereich. Die betroffenen Patienten haben Probleme beim Gehen. Sie sind unsicher und stolpern häufig. Schnelles Laufen ist nicht möglich. Aufgrund der Schwäche der Oberschenkelmuskulatur können sich die Patienten kaum noch alleine aufrichten. Aus diesem Grund stützen sie sich beim Aufrichten mit den Händen am Oberschenkel ab, was auch als Gowers-Zeichen bezeichnet wird. Da die Muskeldystrophie Typ Duchenne vor allem im Bereich der Waden zu einer Zunahme des Fettgewebes und des Bindegewebes führt, erscheinen diese sehr kräftig. Man spricht auch von Gnomenwaden. Zusätzlich werden häufig eine ausgeprägte Lendenlordose und Spitzfüße beobachtet. Die Erkrankung zeigt einen rasch progredienten Verlauf. Im Laufe der Zeit führt die Erkrankung auch zu einer Muskelschwäche und Muskelatrophie an der oberen Extremität mit Scapula alata. Die meisten Patienten sitzen zum Zeitpunkt des 12. Lebensjahres im Rollstuhl. Die Rollstuhlabhängigkeit führt zu einer progredienten Skoliose mit Reduktion der Vitalkapazität. Zusätzlich schränkt eine Schwäche der Atemmuskulatur die Atmung weiter ein.
Wenn die Patienten das zehnte Lebensjahr überschritten haben, wird die zuvor präklinische Kardiomyopathie klinisch relevant. Jeder dritte Patient weist eine Intelligenzminderung auf.
In einem fortgeschrittenen Stadium kommt es zu einer Areflexie. Faszikulationen, Fibrillationen und Sensibilitätsstörungen werden nicht beobachtet. Die Lebenserwartung beträgt ca. 40 Jahre,wobei aber auch vile Patienten bereits im Kindesalter versterben.
Eteplirsen wurde von Sarepta Therapeutics zur Behandlung von Duchenne in der Klinik getestet und befindet sich derzeit im Zulassungsprozedere der amerikanischen Arzneimittelbehörde (FDA). Eine von der FDA einberufene Expertenrunde hat mit 7:6 gegen eine Zulassung gestimmt. Der Zulassungsantrag beruht auf sehr schwachen klinischen Daten, so dass die FDA von 13 Patienten eine Biopsie zum Nachweis von Dystrophin in den Muskelpartien als Folge der Behandlung mit Eteplirsen eingefordert hat.
Unter normalen Umständen hätte dieser Zulassungsantrag keine Chance auf einen positiven Bescheid. In Anbetracht der nicht vorhandenen Therapiemöglichkeiten und dem grausamen Krankheitsverlauf, ist - positive Biopsieergebnisse vorausgesetzt- die Zulassung im Sommer 2016 dennoch nicht ausgeschlossen. Bei ungünstigen Bipsieergebnissen (kein Nachweis von Dystrophin) erfolgt ein Absturz sehr wahrscheinlich unter 5$.
Ich habe mir Heute eine kleine Position zu USD 18.88 ins Depot gelegt und habe diese sofort abgeschrieben!
ACHTUNG: HOCHSPEKULATIV!
Deswegen nur bedingt zur Nachahmung empfohlen! Höchstens Reserven investieren, die SOFORT abgeschrieben werden können. TOTALVERLUST möglich.
Sollte Eteplirsen allerdings zugelassen werden, dann sind dreistellige Kurse aufgrund des Alleinstellungsmerkmales wahrscheinlich.
Antwort auf Beitrag Nr.: 52.573.682 von cyberhexe123 am 08.06.16 22:57:18Danke für Deinen Beitrag.
Soviel zum Thema dreistellige Kurse ;-)
Sehe es aber ähnlich wie Du - momentan unter $ 40 USD wirklich free money - Meinungen?
Viele Grüße
Soviel zum Thema dreistellige Kurse ;-)
Sehe es aber ähnlich wie Du - momentan unter $ 40 USD wirklich free money - Meinungen?
Viele Grüße
Antwort auf Beitrag Nr.: 53.690.451 von biopadawan am 14.11.16 16:33:04da eine Zulassung alles andere als eine ausgemachte Angelegenheit war, hatte ich vor der Zulassungsentscheidung lediglich eine kleine Position aufgebaut. Aber nun, bei Kursen unter USD40, stimme ich dir zu, könnte man über einen Ausbau der Position nachdenken. Werde einen Kaufauftrag bei ca. USD 36 positionieren.
Antwort auf Beitrag Nr.: 53.690.451 von biopadawan am 14.11.16 16:33:04
Da würde ich aber zur gegenwärtigen Bewertung Santhera vorziehen!!
Zitat von biopadawan: Danke für Deinen Beitrag.
Soviel zum Thema dreistellige Kurse ;-)
Sehe es aber ähnlich wie Du - momentan unter $ 40 USD wirklich free money - Meinungen?
Viele Grüße
Da würde ich aber zur gegenwärtigen Bewertung Santhera vorziehen!!
Antwort auf Beitrag Nr.: 53.702.553 von Cyberhexe am 16.11.16 06:39:33
Und gekauft gestern?
Zitat von Cyberhexe: da eine Zulassung alles andere als eine ausgemachte Angelegenheit war, hatte ich vor der Zulassungsentscheidung lediglich eine kleine Position aufgebaut. Aber nun, bei Kursen unter USD40, stimme ich dir zu, könnte man über einen Ausbau der Position nachdenken. Werde einen Kaufauftrag bei ca. USD 36 positionieren.
Und gekauft gestern?
Antwort auf Beitrag Nr.: 53.808.690 von Gustl24 am 01.12.16 14:53:57Natürlich !!!!
Antwort auf Beitrag Nr.: 53.887.685 von biopadawan am 13.12.16 22:43:50Aktuell sehr billig zu haben.
na die saust in schwindelnen Höhen, sowas würde ich gerne mal wieder bei Santhera sehen.
Antwort auf Beitrag Nr.: 54.051.601 von mfierke am 10.01.17 17:55:37Wird schön unten gehalten das ding
Ist noch jemand investiert?
Ist noch jemand investiert?
Bin auch dabei. 
Die ersten Umsätze waren vielversprechend. Sie haben zwar nur eine provisorische Zulassung, aber dafür praktisch keine Konkurrenz. Biomarin ist gescheitert, PTC macht mickrige Umsätze in Europa, in den USA wurden sie zurückgewiesen. Und Santhera spielt bisschen am Rand mit.

Die ersten Umsätze waren vielversprechend. Sie haben zwar nur eine provisorische Zulassung, aber dafür praktisch keine Konkurrenz. Biomarin ist gescheitert, PTC macht mickrige Umsätze in Europa, in den USA wurden sie zurückgewiesen. Und Santhera spielt bisschen am Rand mit.
Antwort auf Beitrag Nr.: 54.214.597 von paul81 am 01.02.17 15:46:37Sarepta wird am 19.7. die Quartalszahlen bekanntgeben, wobei mit Hochspannung der Umsatz für Exondys 51 erwartet wird: Konsens bei den Analysten ist ein Umsatz von $22.3m nach $16.3m im 1. Quartal.
Ich rechne mit $25m!
Ich rechne mit $25m!
Danke Cyberhexe
Habe Sarepta schon länger auf meiner Watchlist, das Datum hatte ich aber nicht mehr im Kopf.
Habe Sarepta schon länger auf meiner Watchlist, das Datum hatte ich aber nicht mehr im Kopf.
Antwort auf Beitrag Nr.: 55.327.444 von Cyberhexe am 14.07.17 18:59:59
...da war meine Schätzung noch zu konservativ:
"Sarepta shoots higher as sales of $300,000-a-year drug exceed expectations
Published: July 19, 2017 5:37 p.m. ET
Sarepta Therapeutics Inc. SRPT, +0.56% shares shot more than 13% higher in late trading Wednesday after the company reported sales of its $300,000-a-year drug for Duchenne muscular dystrophy were better than expected. Sarepta announced second-quarter revenue of $35 million, easily beating the average analyst forecast of $22.5 million, according to a FactSet survey. The company brought in nearly as much in sales during the second quarter as it did in the previous six fiscal years, when it recorded $36 million in revenue amid a nearly decade-long effort to get FDA approval for eteplirsen, the first approved treatment for DMD. Sarepta also increased its forecast for full-year revenue, to a range of $125 million to $130 million from previous guidance of more than $95 million. Sarepta stock rose to about $38.80 in late trading, after closing with a 0.6% gain at $34.08; the stock is up more than 61% in the past year, as the S&P 500 index SPX, +0.54% has gained 13.7%."
Zitat von Cyberhexe: Sarepta wird am 19.7. die Quartalszahlen bekanntgeben, wobei mit Hochspannung der Umsatz für Exondys 51 erwartet wird: Konsens bei den Analysten ist ein Umsatz von $22.3m nach $16.3m im 1. Quartal.
Ich rechne mit $25m!
...da war meine Schätzung noch zu konservativ:
"Sarepta shoots higher as sales of $300,000-a-year drug exceed expectations
Published: July 19, 2017 5:37 p.m. ET
Sarepta Therapeutics Inc. SRPT, +0.56% shares shot more than 13% higher in late trading Wednesday after the company reported sales of its $300,000-a-year drug for Duchenne muscular dystrophy were better than expected. Sarepta announced second-quarter revenue of $35 million, easily beating the average analyst forecast of $22.5 million, according to a FactSet survey. The company brought in nearly as much in sales during the second quarter as it did in the previous six fiscal years, when it recorded $36 million in revenue amid a nearly decade-long effort to get FDA approval for eteplirsen, the first approved treatment for DMD. Sarepta also increased its forecast for full-year revenue, to a range of $125 million to $130 million from previous guidance of more than $95 million. Sarepta stock rose to about $38.80 in late trading, after closing with a 0.6% gain at $34.08; the stock is up more than 61% in the past year, as the S&P 500 index SPX, +0.54% has gained 13.7%."
habe meine position bei sarepta nochmals bisschen aufgestockt
neue resultate haben die positive und statistisch höchst signifikante wirkung auf die dystrophinproduktion durch die behandlung bestätigt:
https://seekingalpha.com/news/3293771-sareptas-golodirsen-sh…
exondys 51 wird wohl den erfolgreichsten start einer behandlung bei ultra-seltenen krankheiten hinlegen, und das obwohl die behandlung aktuell nur für 13% der dmd-erkrankten zugelassen ist
ausserdem wird schon an einer verbesserten version des medikaments, mit einer um ein mehrfaches stärkeren wirkung gearbeitet (pmo vs ppmo)... vom CEO aus dem transkript einer konferenz:
"Well, we're really excited. I get accused of being maybe overly excited about PPMO science, but it could be a significant life-altering therapy if it works the way we imagine it. So our PMO technology does things - it's brilliant. It is precision medicine. When it gets into the cell, it creates exon skipping, which means it literally excises an exon at the pre-messenger RNA level and creates the right - and it skips messenger RNA and then creates dystrophin and then it looks like it's localizing in the right way. So it is doing everything it's supposed to do, and the challenge with the PMO is how to get enough of it into the cell. So as it stands right now, a lot of it's not getting into the cell because it's neutrally charged. The beauty of PPMO is it's essentially - with 51, it's the same sequence with a conjugated peptide.
And with that conjugated peptide, at least in animal models, you can get as much as an order of magnitude more dystrophin production. So it would be extraordinarily significant if it works. The issue that we're looking at right now, our goal right now is to be - to have a first patient in on a trial for a PPMO this year. But we're waiting for the talks. We have the nonhuman primate talks data, that 13-week data that will be coming in any day now, and if that looks good, we'll file an IND and once approved, we'll announce all that, and we'll be first patient in this year on PPMO. And if it works, and if we're able to dose it to therapeutic levels, it could really be a significant game changer for the treatment of DMD."
vollständiges transkript:
https://seekingalpha.com/article/4106686-sarepta-therapeutic…
wen es interessiert kann es auch etwas ausführlicher beschrieben in diesem transkript einer anderen konferenz nachlesen (stichwort "ppmo"):
https://seekingalpha.com/article/4106825-sarepta-therapeutic…
dazu kommen noch diverse partnerschaften (z.b. mit summit http://www.summitplc.com/programmes/duchenne-muscular-dystro…), die die vorherrschaft bei der dmd-behandlung auch in zukunft sicherstellen sollen
das einzige was die aktien bzw. den kurs bremst ist die bedingte zulassung durch die fda
wenn alles gut geht, sprich die defintive zulassung erhalten wird, könnte das meiner meinung nach die nächste alexion werden, sie haben aktuell keine konkurrenz bei dmd
neue resultate haben die positive und statistisch höchst signifikante wirkung auf die dystrophinproduktion durch die behandlung bestätigt:
https://seekingalpha.com/news/3293771-sareptas-golodirsen-sh…
exondys 51 wird wohl den erfolgreichsten start einer behandlung bei ultra-seltenen krankheiten hinlegen, und das obwohl die behandlung aktuell nur für 13% der dmd-erkrankten zugelassen ist
ausserdem wird schon an einer verbesserten version des medikaments, mit einer um ein mehrfaches stärkeren wirkung gearbeitet (pmo vs ppmo)... vom CEO aus dem transkript einer konferenz:
"Well, we're really excited. I get accused of being maybe overly excited about PPMO science, but it could be a significant life-altering therapy if it works the way we imagine it. So our PMO technology does things - it's brilliant. It is precision medicine. When it gets into the cell, it creates exon skipping, which means it literally excises an exon at the pre-messenger RNA level and creates the right - and it skips messenger RNA and then creates dystrophin and then it looks like it's localizing in the right way. So it is doing everything it's supposed to do, and the challenge with the PMO is how to get enough of it into the cell. So as it stands right now, a lot of it's not getting into the cell because it's neutrally charged. The beauty of PPMO is it's essentially - with 51, it's the same sequence with a conjugated peptide.
And with that conjugated peptide, at least in animal models, you can get as much as an order of magnitude more dystrophin production. So it would be extraordinarily significant if it works. The issue that we're looking at right now, our goal right now is to be - to have a first patient in on a trial for a PPMO this year. But we're waiting for the talks. We have the nonhuman primate talks data, that 13-week data that will be coming in any day now, and if that looks good, we'll file an IND and once approved, we'll announce all that, and we'll be first patient in this year on PPMO. And if it works, and if we're able to dose it to therapeutic levels, it could really be a significant game changer for the treatment of DMD."
vollständiges transkript:
https://seekingalpha.com/article/4106686-sarepta-therapeutic…
wen es interessiert kann es auch etwas ausführlicher beschrieben in diesem transkript einer anderen konferenz nachlesen (stichwort "ppmo"):
https://seekingalpha.com/article/4106825-sarepta-therapeutic…
dazu kommen noch diverse partnerschaften (z.b. mit summit http://www.summitplc.com/programmes/duchenne-muscular-dystro…), die die vorherrschaft bei der dmd-behandlung auch in zukunft sicherstellen sollen
das einzige was die aktien bzw. den kurs bremst ist die bedingte zulassung durch die fda
wenn alles gut geht, sprich die defintive zulassung erhalten wird, könnte das meiner meinung nach die nächste alexion werden, sie haben aktuell keine konkurrenz bei dmd
keine konkurrenz in sicht
nach santhera wird nun wohl auch ptc therapeutics zum wiederholten mal die zulassung verweigert... keine konkurrenz in sicht für sarepta
Nächste Woche wird ja Sarepta zusammen mit Catabasis neue Daten präsentieren...
Warum krallt sich Sarepta nicht gleich Catabasis? Wäre doch (noch?) ein Schnäppchen und aus der Portokasse zu bezahlen?!
Warum krallt sich Sarepta nicht gleich Catabasis? Wäre doch (noch?) ein Schnäppchen und aus der Portokasse zu bezahlen?!
Bin seit 02/2016 in SRPT dabei. Hatte mir eine Menge Aktien zugelegt, die ich in 10/2016 überaus erfolgreich verkaufen konnte. Im Frühjahr dann der Wiedereinstieg. Ich bin ziemlich überzeugt davon, dass wir bei SRPT einen 3-stelligen Kurs (in USD) erleben werden. Gehe dabei von 1 HJ 2018 aus. Eine derzeit mögliche vorzeitige Zulassung von Exondys 53/45 in den USA , Zulassung Exondys 51 in der EU und ein Verkauf der Firma an einen Branchenriesen lassen mich von deutlich höheren Kursen träumen.
Antwort auf Beitrag Nr.: 56.029.329 von paul81 am 26.10.17 09:06:55....nicht schlecht:
Net Revenues
For the third quarter of 2017, the Company recognized net revenues of $46.0 million which reflects sales
from EXONDYS 51 in the U.S. No revenue was recognized for the same period of 2016.
Net Revenues
For the third quarter of 2017, the Company recognized net revenues of $46.0 million which reflects sales
from EXONDYS 51 in the U.S. No revenue was recognized for the same period of 2016.
Antwort auf Beitrag Nr.: 55.965.492 von chippi2710 am 17.10.17 13:47:14
...das bin ich auch!
Bin bei Threaderöffnung jedoch eher vorsichtig eingestiegen (700 Stück, da hochspekulativ!) - werde jedoch mindestens eine Vervierfachung abwarten, bevor die ersten Teile verkauft werden!
Zitat von chippi2710: Bin seit 02/2016 in SRPT dabei. Hatte mir eine Menge Aktien zugelegt, die ich in 10/2016 überaus erfolgreich verkaufen konnte. Im Frühjahr dann der Wiedereinstieg. Ich bin ziemlich überzeugt davon, dass wir bei SRPT einen 3-stelligen Kurs (in USD) erleben werden. Gehe dabei von 1 HJ 2018 aus. Eine derzeit mögliche vorzeitige Zulassung von Exondys 53/45 in den USA , Zulassung Exondys 51 in der EU und ein Verkauf der Firma an einen Branchenriesen lassen mich von deutlich höheren Kursen träumen.
...das bin ich auch!
Bin bei Threaderöffnung jedoch eher vorsichtig eingestiegen (700 Stück, da hochspekulativ!) - werde jedoch mindestens eine Vervierfachung abwarten, bevor die ersten Teile verkauft werden!
nicht übel
damit will man sich auch die zukünftige vorherrschaft bei der behandlung von dmd sichern:http://investorrelations.sarepta.com/news-releases/news-rele…
und noch eine schöne aktuelle präsentation hinterher:
http://investorrelations.sarepta.com/static-files/55591721-d…
http://investorrelations.sarepta.com/static-files/55591721-d…
Ich glaube ... den geduldigen SRPT Shareholdern steht ein ertragreiches Jahr bevor. :-) Alle Zeichen sprechen aktuell dafür. Good luck!
Läuft :-) ... eine echte Perle kann das noch werden!
Antwort auf Beitrag Nr.: 57.217.489 von chippi2710 am 07.03.18 22:35:05...und läuft und läuft und läuft: die wahrscheinliche Empfehlung des europ. Arzneimittelausschusses CHMP zur Zulassung SRPTs Gentherapie bei Duchenne wird das Potenzial des Unternehmens noch einmal verdoppeln - der Tenbagger ist nicht mehr unrealistisch!
Antwort auf Beitrag Nr.: 57.243.280 von Cyberhexe am 10.03.18 16:59:20Für eine Aktie mit dem Potenzial wie es Sarepta Therapeutics hat, ist hier ganz schön wenig los. Heute ein weiterer Meilenstein ....
Sarepta Therapeutics Announces Plan to Submit a New Drug Application (NDA) for Accelerated Approval of Golodirsen (SRP-4053) in Patients with Duchenne Muscular Dystrophy (DMD) Amenable to Skipping Exon 53
March 12, 2018 at 7:30 AM EDT
Sarepta Therapeutics Announces Plan to Submit a New Drug Application (NDA) for Accelerated… Approval of Golodirsen (SRP-4053) in Patients with Duchenne Muscular Dystrophy (DMD) Amenable to Skipping Exon 53
-- The Company met with the FDA Division of Neurology Products in February to obtain guidance on the regulatory pathway for golodirsen --
-- The Company intends to complete a rolling NDA submission for golodirsen by year-end 2018 --
CAMBRIDGE, Mass., March 12, 2018 (GLOBE NEWSWIRE) -- Sarepta Therapeutics, Inc. (NASDAQ:SRPT), a commercial-stage biopharmaceutical company focused on the discovery and development of precision genetic medicine to treat rare neuromuscular diseases, announced today that it recently received final minutes from a February 2018 Type C meeting held with the Division of Neurology Products, United States Food and Drug Administration (the Division), to solicit the Division's guidance on the development pathway for Sarepta's therapeutic candidate, golodirsen, a phosphordiamidate morpholino oligimer engineered to treat those patients with Duchenne muscular dystrophy (DMD) who have genetic mutations subject to skipping exon 53 of the DMD gene.
"Sarepta is thankful for the FDA Neurology Division’s thoughtful and direct guidance regarding golodirsen," said Doug Ingram, Sarepta's president and chief executive officer. "Obviously, whether golodirsen will obtain accelerated approval is a review decision that will come after the submission and review of our NDA. But we greatly appreciate the willingness of the Neurology Division to engage and provide clear direction to us on the steps necessary to support an NDA submission for accelerated approval."
Sarepta Therapeutics Announces Plan to Submit a New Drug Application (NDA) for Accelerated Approval of Golodirsen (SRP-4053) in Patients with Duchenne Muscular Dystrophy (DMD) Amenable to Skipping Exon 53
March 12, 2018 at 7:30 AM EDT
Sarepta Therapeutics Announces Plan to Submit a New Drug Application (NDA) for Accelerated… Approval of Golodirsen (SRP-4053) in Patients with Duchenne Muscular Dystrophy (DMD) Amenable to Skipping Exon 53
-- The Company met with the FDA Division of Neurology Products in February to obtain guidance on the regulatory pathway for golodirsen --
-- The Company intends to complete a rolling NDA submission for golodirsen by year-end 2018 --
CAMBRIDGE, Mass., March 12, 2018 (GLOBE NEWSWIRE) -- Sarepta Therapeutics, Inc. (NASDAQ:SRPT), a commercial-stage biopharmaceutical company focused on the discovery and development of precision genetic medicine to treat rare neuromuscular diseases, announced today that it recently received final minutes from a February 2018 Type C meeting held with the Division of Neurology Products, United States Food and Drug Administration (the Division), to solicit the Division's guidance on the development pathway for Sarepta's therapeutic candidate, golodirsen, a phosphordiamidate morpholino oligimer engineered to treat those patients with Duchenne muscular dystrophy (DMD) who have genetic mutations subject to skipping exon 53 of the DMD gene.
"Sarepta is thankful for the FDA Neurology Division’s thoughtful and direct guidance regarding golodirsen," said Doug Ingram, Sarepta's president and chief executive officer. "Obviously, whether golodirsen will obtain accelerated approval is a review decision that will come after the submission and review of our NDA. But we greatly appreciate the willingness of the Neurology Division to engage and provide clear direction to us on the steps necessary to support an NDA submission for accelerated approval."
Antwort auf Beitrag Nr.: 57.253.303 von chippi2710 am 12.03.18 15:01:10Barclays hat das Kursziel auf $107 erhöht:
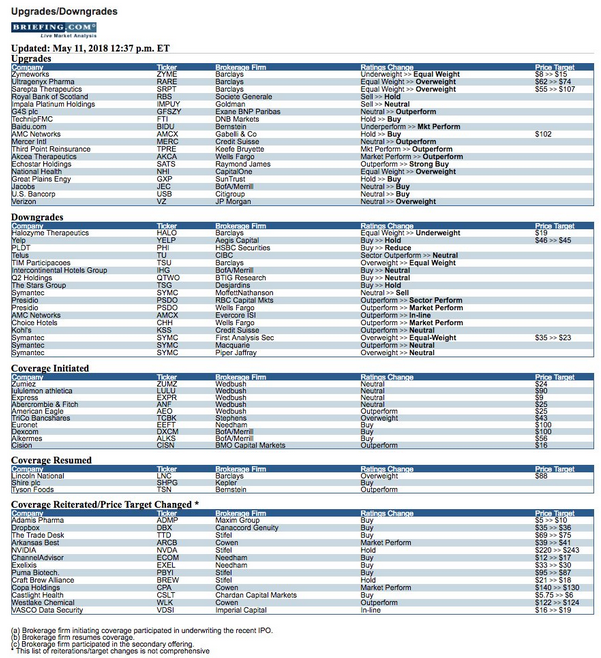

06/6/18
9:00 AM EDT
Sarepta Therapeutics Inc. Annual Meeting of Stockholders
The meeting will be held at the Company’s headquarters, 215 First Street, Suite 110B, Cambridge, MA 02142.
9:00 AM EDT
Sarepta Therapeutics Inc. Annual Meeting of Stockholders
The meeting will be held at the Company’s headquarters, 215 First Street, Suite 110B, Cambridge, MA 02142.
Antwort auf Beitrag Nr.: 57.879.597 von Cyberhexe am 31.05.18 17:52:50
Sarepta --> Nomura. Reiterates a Buy, PT $131 #DMD
Sarepta --> Nomura. Reiterates a Buy, PT $131 #DMD
Antwort auf Beitrag Nr.: 57.911.955 von Cyberhexe am 05.06.18 15:07:14Kurs ist nun dreistellig!
Sarepta Therapeutics Enters into Long-term Strategic Manufacturing Partnership with Brammer Bio to Support Gene Therapy Development and Commercial Supply
June 13, 2018 at 8:30 AM EDT
Sarepta Therapeutics Enters into Long-term Strategic Manufacturing Partnership with Brammer Bio to Support Gene Therapy Development and Commercial Supply
-- The partnership will provide commercial supply for a potential micro-dystrophin gene therapy product launch and other neuromuscular programs in the pipeline --
-- Hybrid model enables Sarepta to maintain control over process development, while leveraging Brammer Bio’s world-class manufacturing capabilities --
Sarepta Therapeutics Enters into Long-term Strategic Manufacturing Partnership with Brammer Bio to Support Gene Therapy Development and Commercial Supply
June 13, 2018 at 8:30 AM EDT
Sarepta Therapeutics Enters into Long-term Strategic Manufacturing Partnership with Brammer Bio to Support Gene Therapy Development and Commercial Supply
-- The partnership will provide commercial supply for a potential micro-dystrophin gene therapy product launch and other neuromuscular programs in the pipeline --
-- Hybrid model enables Sarepta to maintain control over process development, while leveraging Brammer Bio’s world-class manufacturing capabilities --
Antwort auf Beitrag Nr.: 55.965.492 von chippi2710 am 17.10.17 13:47:14Ja, nun ist es passiert. Der Kurs ist 3-stellig  . Lag mit meiner Vermutung vom 17.10.17 gar nicht nso falsch. Allerdings hatte ich Sachverhalte einbezogen, die bisher noch nicht eingetroffen sind.
. Lag mit meiner Vermutung vom 17.10.17 gar nicht nso falsch. Allerdings hatte ich Sachverhalte einbezogen, die bisher noch nicht eingetroffen sind.
- Euro-Zulassung (bisher eine negative Entscheidung)
- Zulassung von Exondys 53/45 (Entscheidung wohl erst in 2019)
- Übernahme durch Branchenriesen
Und jetzt kann es ganz schnell gehen und wir sind bei Kursen von USD 120 oder höher. Morgen spricht Doug Ingram beim R&D day über die Entwicklungen und Ergebnisse der medizinischen Versuche. Diese scheinen ziemlich vielverbrechend zu sein.
Mittlerweile hat sich Sarepta zu einer Multi-rare-neuromuscular-diseases Plattform gemausert. Neue Therapiefelder wurden aufgetan und wichtige strategische Partnerschaften eingegangen. Sogar die Übernahme eines anderen Biopharma-Unternehmens ist vertraglich festgelegt. Der Wechsel zum neuen CEO Douglas Ingram in 2017 hat sich als Königstransfer herausgestellt. Weitere kluge Personalentscheidungen sind auch getroffen.
Langfristig sehe ich den Kurs in 06/2019 bei USD 250 :Eck: und in 5 Jahren (wenn SRPT nicht übernommen wird) bei USD 500+ .
.
Ich bleibe long ....
 . Lag mit meiner Vermutung vom 17.10.17 gar nicht nso falsch. Allerdings hatte ich Sachverhalte einbezogen, die bisher noch nicht eingetroffen sind.
. Lag mit meiner Vermutung vom 17.10.17 gar nicht nso falsch. Allerdings hatte ich Sachverhalte einbezogen, die bisher noch nicht eingetroffen sind. - Euro-Zulassung (bisher eine negative Entscheidung)
- Zulassung von Exondys 53/45 (Entscheidung wohl erst in 2019)
- Übernahme durch Branchenriesen
Und jetzt kann es ganz schnell gehen und wir sind bei Kursen von USD 120 oder höher. Morgen spricht Doug Ingram beim R&D day über die Entwicklungen und Ergebnisse der medizinischen Versuche. Diese scheinen ziemlich vielverbrechend zu sein.
Mittlerweile hat sich Sarepta zu einer Multi-rare-neuromuscular-diseases Plattform gemausert. Neue Therapiefelder wurden aufgetan und wichtige strategische Partnerschaften eingegangen. Sogar die Übernahme eines anderen Biopharma-Unternehmens ist vertraglich festgelegt. Der Wechsel zum neuen CEO Douglas Ingram in 2017 hat sich als Königstransfer herausgestellt. Weitere kluge Personalentscheidungen sind auch getroffen.
Langfristig sehe ich den Kurs in 06/2019 bei USD 250 :Eck: und in 5 Jahren (wenn SRPT nicht übernommen wird) bei USD 500+
 .
. Ich bleibe long ....
Zitat von chippi2710: Bin seit 02/2016 in SRPT dabei. Hatte mir eine Menge Aktien zugelegt, die ich in 10/2016 überaus erfolgreich verkaufen konnte. Im Frühjahr dann der Wiedereinstieg. Ich bin ziemlich überzeugt davon, dass wir bei SRPT einen 3-stelligen Kurs (in USD) erleben werden. Gehe dabei von 1 HJ 2018 aus. Eine derzeit mögliche vorzeitige Zulassung von Exondys 53/45 in den USA , Zulassung Exondys 51 in der EU und ein Verkauf der Firma an einen Branchenriesen lassen mich von deutlich höheren Kursen träumen.
Wow ... Hammer ... bin völlig geflasht. Noch ist der Handel von SRPT ausgesetzt. Die verkündeten Ergebnisse auf dem R & D day sind gigantisch! Wo endet der Kurs nach der Handelsaussetzung heute?
$170 - Hexe ... Dein 10-bagger ist bald geschafft! 





viel zu früh raus, ätzend 
Biotechs für kleine Gewinne traden bringts, für mich zumindest, nicht... GRATULIERE allen Investierten

Biotechs für kleine Gewinne traden bringts, für mich zumindest, nicht... GRATULIERE allen Investierten

Antwort auf Beitrag Nr.: 58.019.560 von chippi2710 am 19.06.18 17:13:16
not too bad:
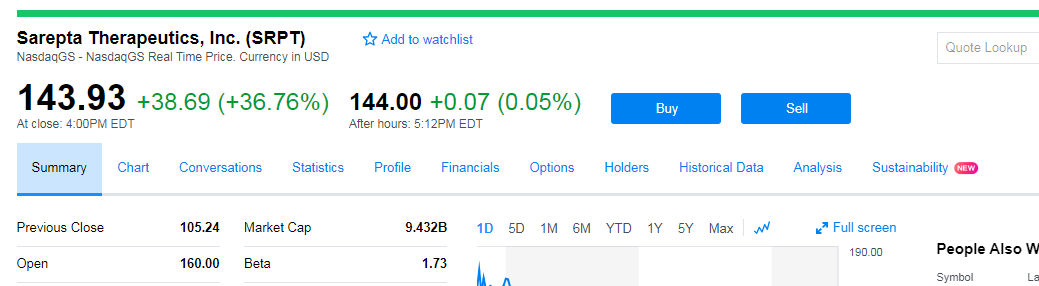
Zitat von chippi2710: $170 - Hexe ... Dein 10-bagger ist bald geschafft!
not too bad:

Antwort auf Beitrag Nr.: 58.022.119 von Cyberhexe am 19.06.18 23:39:49Auf der Grundlage der bisher berichteten Ergebnisse erweitert Sarepta die derzeit kleine klinische Einarmstudie in eine größere Studie, in der mehr Duchenne-Patienten und ein Placebo-Arm eingeschlossen werden. Die in Cambridge, Massachusetts, ansässige Biotech-Firma beabsichtigt, sich mit der FDA zu treffen, um zu zeigen, dass diese erweiterte Studie ausreichen sollte, um eine Marktzulassung zu beantragen, vorausgesetzt die Daten sind positiv, sagte Doug Ingram, CEO von Sarepta.
In der am Dienstag vorgestellten klinischen Studie erhielten drei Jungen mit Duchenne im Alter von 4, 5 und 6 Jahren im Januar, Februar und März jeweils eine einzige Injektion der Mikrodystrophin-Gentherapie. Nach drei Monaten Follow-up für jeden Jungen wurden Muskelbiopsien durchgeführt und mit Biopsien zu Beginn der Studie verglichen.
Das Ergebnis: Nach drei Monaten produzierten die Jungen ein durchschnittliches Niveau von Mikrodystrophin, das 38,2 Prozent der normalen Werte betrug, wie durch einen Western-Blot-Test gemessen wurde.
Wie gut ist das Ergebnis? Es ist fast viermal besser als erwartet, sagte Ingram.
Dr. John Day, Direktor der neuromuskulären Medizin an der Medizinischen Fakultät der Stanford University,wird mit den folgenden euphorischen Worten zitiert:
"... dies sind wahrscheinlich die positivsten Ergebnisse, die man zu diesem Zeitpunkt erwarten konnte".
In der am Dienstag vorgestellten klinischen Studie erhielten drei Jungen mit Duchenne im Alter von 4, 5 und 6 Jahren im Januar, Februar und März jeweils eine einzige Injektion der Mikrodystrophin-Gentherapie. Nach drei Monaten Follow-up für jeden Jungen wurden Muskelbiopsien durchgeführt und mit Biopsien zu Beginn der Studie verglichen.
Das Ergebnis: Nach drei Monaten produzierten die Jungen ein durchschnittliches Niveau von Mikrodystrophin, das 38,2 Prozent der normalen Werte betrug, wie durch einen Western-Blot-Test gemessen wurde.
Wie gut ist das Ergebnis? Es ist fast viermal besser als erwartet, sagte Ingram.
Dr. John Day, Direktor der neuromuskulären Medizin an der Medizinischen Fakultät der Stanford University,wird mit den folgenden euphorischen Worten zitiert:
"... dies sind wahrscheinlich die positivsten Ergebnisse, die man zu diesem Zeitpunkt erwarten konnte".
Antwort auf Beitrag Nr.: 58.022.146 von Cyberhexe am 19.06.18 23:52:45
Sarepta Therapeutics (NASDAQ:SRPT) Rating Reaffirmed
New York: In analysts note shared with investors on Wednesday morning, Morgan Stanley restate their “Equal-Weight” rating on Sarepta Therapeutics (NASDAQ:SRPT) shares. They now have a $163 target price on the company. Morgan Stanley’s target would indicate a potential upside of 6.06 % from the company’s current stock price.
Sarepta Therapeutics (NASDAQ:SRPT) Rating Reaffirmed
New York: In analysts note shared with investors on Wednesday morning, Morgan Stanley restate their “Equal-Weight” rating on Sarepta Therapeutics (NASDAQ:SRPT) shares. They now have a $163 target price on the company. Morgan Stanley’s target would indicate a potential upside of 6.06 % from the company’s current stock price.
Antwort auf Beitrag Nr.: 58.034.494 von Cyberhexe am 21.06.18 13:12:01Duchenne wird durch eine vererbte Mutation in einem Gen verursacht, das Dystrophin produziert, ein Protein, das für die Steuerung der Muskeln benötigt wird. Ohne Dystrophin sind die Muskeln mit der Zeit nicht mehr erregbar, weshalb Duchenne-Patienten nach und nach ihre Gehfähigkeit verlieren. Die Krankheit verläuft bisher für die betroffenen Jungen (da X-chromosomal) tödlich - meistens im späten Teenager-Alter oder Anfang 20.
Sareptas GENTHERAPIE zur Behandlung von Duchenne führt zu einer beachtlichen Produktion des fehlenden Muskelproteins. Die neusten Ergebnisse sind zwar nur auf die Auswertung von 3 therapierten Jungen basiert, deuten jedoch daraufhin, dass der Krankheitsverlauf bei denn Duchenne-Kindern gestoppt werden kann bzw. sogar umkehrbar ist.
Sareptas GENTHERAPIE zur Behandlung von Duchenne führt zu einer beachtlichen Produktion des fehlenden Muskelproteins. Die neusten Ergebnisse sind zwar nur auf die Auswertung von 3 therapierten Jungen basiert, deuten jedoch daraufhin, dass der Krankheitsverlauf bei denn Duchenne-Kindern gestoppt werden kann bzw. sogar umkehrbar ist.
Antwort auf Beitrag Nr.: 58.040.422 von Cyberhexe am 22.06.18 06:27:03Dies sind natürlich schlechte Nachrichten. Das Unternehmen wird bemüht sein, die Qualitätsprobleme so schnell wie möglich zu beheben.
Sarepta Therapeutics’ clinical trial for a gene therapy to treat Duchenne muscular dystrophy has been paused by the Food and Drug Administration because some of the materials used in the treatment weren’t as they should be, the company announced Wednesday.
A stray DNA fragment was found “in connection with routine quality assurance testing” of the plasmids used in the company’s gene therapy, said Douglas Ingram, Sarepta’s president and CEO. Plasmids carry the genetic material used in gene therapy into a cell. The FDA notified Nationwide Children’s Research Institute, where the trial is being conducted, of the clinical hold on Tuesday.
Sarepta Therapeutics’ clinical trial for a gene therapy to treat Duchenne muscular dystrophy has been paused by the Food and Drug Administration because some of the materials used in the treatment weren’t as they should be, the company announced Wednesday.
A stray DNA fragment was found “in connection with routine quality assurance testing” of the plasmids used in the company’s gene therapy, said Douglas Ingram, Sarepta’s president and CEO. Plasmids carry the genetic material used in gene therapy into a cell. The FDA notified Nationwide Children’s Research Institute, where the trial is being conducted, of the clinical hold on Tuesday.
Antwort auf Beitrag Nr.: 58.407.258 von Cyberhexe am 09.08.18 09:43:56Sarepta's frühe klinische Studie bei der gentherapeutischen Behandlung der Duchenne-Muskeldystrophie ist wieder im Zeitplan, vermeldete das Unternehmen Montag an. DieFDA hatte die Studie im Juli auf Eis gelegt.
Die FDA ordnete den Halt an, nachdem bei der Behandlung kleine DNA-Fragmente aufgetaucht sind. Die kontaminierte Charge wurde nie bei Patienten verwendet, aber das Unternehmen sagte, dass es zu einer höheren Qualität von Plasmiden wechseln würde. Sarepta-Sprecher Ian Estepan bestätigte, dass die neuen Plasmide vom gleichen Lieferanten kommen.
Die Behandlung soll die Menge eines Proteins namens Microdystrophin - eine kleinere Version des Dystrophin-Gens, das Menschen mit Duchenne fehlt - im ganzen Körper erhöhen.
Die FDA ordnete den Halt an, nachdem bei der Behandlung kleine DNA-Fragmente aufgetaucht sind. Die kontaminierte Charge wurde nie bei Patienten verwendet, aber das Unternehmen sagte, dass es zu einer höheren Qualität von Plasmiden wechseln würde. Sarepta-Sprecher Ian Estepan bestätigte, dass die neuen Plasmide vom gleichen Lieferanten kommen.
Die Behandlung soll die Menge eines Proteins namens Microdystrophin - eine kleinere Version des Dystrophin-Gens, das Menschen mit Duchenne fehlt - im ganzen Körper erhöhen.
Antwort auf Beitrag Nr.: 58.787.912 von Cyberhexe am 24.09.18 23:36:02In der klinischen Studie zu Beginn dieses Jahres hat eine Gentherapie bei Duchenne-Muskeldystrophie zu einer höheren Konzentration des fehlenden Muskelproteins geführt, welches normalerweise bei Patienten mit Duchenne nicht vorhanden ist.
Die im Juni veröffentlichten Ergebnisse waren besser als erwartet, ließen aber dennoch eine wichtige Frage offen: Würde eine erhöhte Proteinkonzentration zu einer signifikanten Verbesserung der Muskelkraft bewirken?
Die Antwort - allerdings lediglich basierend auf den Daten von nur vier Patienten - ist ein klares Ja.
Alle vier Jungen, die mit der Gentherapie von Sarepta behandelt wurden, zeigten Verbesserungen in Muskelfunktion, Kraft, Gehfähigkeit und Geschicklichkeit. Fünf verschiedene Tests wurden zur Messung der Motorik verwendet, wobei die Nachbeobachtungszeit zwischen drei und neun Monaten dauerte. Die Ergebnisse waren bei ALLEN Tests durchweg positiv.
"Wir wollen sehr vorsichtig sein und diese Ergebnisse wegen des kleinen Datensatzes nicht überbewerten, aber wir denken, dass sie ermutigend sind", sagte Doug Ingram, CEO von Sarepta.
The Research Institute at Nationwide Children's Hospital, will host a webcast conference call from the 23rd International Annual Congress of the World Muscle Society (WMS) in Mendoza, Argentina, on Thursday, October 4, 2018 at 7:00 a.m. Eastern Time / 8:00 a.m. local Argentina time. The call will focus on an update regarding Sarepta’s Duchenne muscular dystrophy (DMD) micro-dystrophin gene therapy program and will be led by Dr. Mendell, a renowned researcher in the field of DMD.
Habe heute 1/3 (also 100 Stück...ja ich weiss, ich war zu wenig mutig!) zum Verkauf gestellt (Ultimo USD 162).
Die im Juni veröffentlichten Ergebnisse waren besser als erwartet, ließen aber dennoch eine wichtige Frage offen: Würde eine erhöhte Proteinkonzentration zu einer signifikanten Verbesserung der Muskelkraft bewirken?
Die Antwort - allerdings lediglich basierend auf den Daten von nur vier Patienten - ist ein klares Ja.
Alle vier Jungen, die mit der Gentherapie von Sarepta behandelt wurden, zeigten Verbesserungen in Muskelfunktion, Kraft, Gehfähigkeit und Geschicklichkeit. Fünf verschiedene Tests wurden zur Messung der Motorik verwendet, wobei die Nachbeobachtungszeit zwischen drei und neun Monaten dauerte. Die Ergebnisse waren bei ALLEN Tests durchweg positiv.
"Wir wollen sehr vorsichtig sein und diese Ergebnisse wegen des kleinen Datensatzes nicht überbewerten, aber wir denken, dass sie ermutigend sind", sagte Doug Ingram, CEO von Sarepta.
The Research Institute at Nationwide Children's Hospital, will host a webcast conference call from the 23rd International Annual Congress of the World Muscle Society (WMS) in Mendoza, Argentina, on Thursday, October 4, 2018 at 7:00 a.m. Eastern Time / 8:00 a.m. local Argentina time. The call will focus on an update regarding Sarepta’s Duchenne muscular dystrophy (DMD) micro-dystrophin gene therapy program and will be led by Dr. Mendell, a renowned researcher in the field of DMD.
Habe heute 1/3 (also 100 Stück...ja ich weiss, ich war zu wenig mutig!) zum Verkauf gestellt (Ultimo USD 162).
Antwort auf Beitrag Nr.: 58.867.395 von Cyberhexe am 04.10.18 11:33:02
Tag 1 JPM19: SAREPTA
Sarepta Therapeutics offered a confusing regulatory update for its microdystrophin gene therapy targeting Duchenne muscular dystrophy (DMD) that raises the risk of a longer-than-expected timeline. The stock fell. The most optimistic approval scenario seems to be off the table: The Food and Drug Administration will not let Sarepta file for approval based only on its current, 24-patient study that uses research-grade product. Instead, the FDA wants the company to conduct another study that will treat DMD patients with its gene therapy manufactured at commercial scale. This “registration” study will start in the back half of the year.
Doug Ingram, Sarepta’s CEO, said the FDA’s conservative stance on gene therapy manufacturing was not a surprise. Sarepta is following the same regulatory path used by AveXis (now Novartis) to submit its spinal muscular atrophy gene therapy for approval, he said. But Ingram isn’t offering firm guidance on when its clinical trial(s) can be completed or how much data the FDA needs to see before allowing a filing. Sarepta might be able to file for FDA approval before the registration study with commercial-supply gene therapy is completed (this is what AveXis/Novartis did) but Ingram won’t commit, pending further FDA discussions. Investors hate uncertainty, even if the long-term story remains strong.
Tag 1 JPM19: SAREPTA
Sarepta Therapeutics offered a confusing regulatory update for its microdystrophin gene therapy targeting Duchenne muscular dystrophy (DMD) that raises the risk of a longer-than-expected timeline. The stock fell. The most optimistic approval scenario seems to be off the table: The Food and Drug Administration will not let Sarepta file for approval based only on its current, 24-patient study that uses research-grade product. Instead, the FDA wants the company to conduct another study that will treat DMD patients with its gene therapy manufactured at commercial scale. This “registration” study will start in the back half of the year.
Doug Ingram, Sarepta’s CEO, said the FDA’s conservative stance on gene therapy manufacturing was not a surprise. Sarepta is following the same regulatory path used by AveXis (now Novartis) to submit its spinal muscular atrophy gene therapy for approval, he said. But Ingram isn’t offering firm guidance on when its clinical trial(s) can be completed or how much data the FDA needs to see before allowing a filing. Sarepta might be able to file for FDA approval before the registration study with commercial-supply gene therapy is completed (this is what AveXis/Novartis did) but Ingram won’t commit, pending further FDA discussions. Investors hate uncertainty, even if the long-term story remains strong.
Antwort auf Beitrag Nr.: 59.579.456 von Cyberhexe am 07.01.19 23:07:09Sarepta Therapeutics (SRPT) veröffentlicht heute ermutigende Ergebnisse einer frühen Studie von seinem zweiten Gentherapieprogramm, das auf eine seltene, muskelzerstörende Krankheit abzielt.
Eine einmalige Infusion eines korrektiven Gens, welches mit einem manipulierten Virus geliefert wird, produzierte aussagekräftige Mengen eines Proteins - durchschnittlich 51 Prozent - wodurch die Muskelfunktion verbessert werden kann, sagt das Unternehmen.
Die drei in der Studie behandelten Patienten haben eine Form der Muskeldystrophie, einer erblichen Erkrankung, die dazu führt, dass die Muskeln um die Hüften und Schultern geschwächt werden und mit der Zeit verkümmern. Mit der Proteinbildung via Genmodifikation hofft man, dieses degenerierenden Prozess aufzuhalten.
Vorbörslich legt SAREPTA zu auf ca. $150!
http://investorrelations.sarepta.com/static-files/1387b1e0-0…
Eine einmalige Infusion eines korrektiven Gens, welches mit einem manipulierten Virus geliefert wird, produzierte aussagekräftige Mengen eines Proteins - durchschnittlich 51 Prozent - wodurch die Muskelfunktion verbessert werden kann, sagt das Unternehmen.
Die drei in der Studie behandelten Patienten haben eine Form der Muskeldystrophie, einer erblichen Erkrankung, die dazu führt, dass die Muskeln um die Hüften und Schultern geschwächt werden und mit der Zeit verkümmern. Mit der Proteinbildung via Genmodifikation hofft man, dieses degenerierenden Prozess aufzuhalten.
Vorbörslich legt SAREPTA zu auf ca. $150!
http://investorrelations.sarepta.com/static-files/1387b1e0-0…
Leider hat Sarepta gestern einen CRL für Golodirsen erhalten:
https://investorrelations.sarepta.com/static-files/94fb2658-…
Jetzt heißt es erst einmal abwarten, welche nächsten Schritte mit der FDA abgesprochen werden.
https://investorrelations.sarepta.com/static-files/94fb2658-…
Jetzt heißt es erst einmal abwarten, welche nächsten Schritte mit der FDA abgesprochen werden.
Antwort auf Beitrag Nr.: 61.296.298 von opportoni am 20.08.19 08:55:25wow...die FDA hat die Entscheidung von August rückgängig gemacht und nun doch das Muskeldystrophie-Medikament von Sarepta Vyondys 53 zur Behandlung von Duchenne überraschend zugelassen. Das hätte ich so nicht erwartet!
Riesiger Deal mit Roche für die Vermarktung der DMD Gene Therapie von Sarepta ausserhalb der USA
upfront $1.15 Mrd., weitere $1.7 Mrd. Meilensteinzahlungen, plus royalties
in der upfront Zahlung ist auch ein Aktienkauf ($400 Mio.) für $158.59 pro Aktie drin
pro Aktie drin
die $200 pro Aktie scheinen nur noch eine Frage der zeit zu sein (wenn nicht was riesig schief geht)
https://investorrelations.sarepta.com/news-releases/news-rel…
upfront $1.15 Mrd., weitere $1.7 Mrd. Meilensteinzahlungen, plus royalties
in der upfront Zahlung ist auch ein Aktienkauf ($400 Mio.) für $158.59
 pro Aktie drin
pro Aktie drindie $200 pro Aktie scheinen nur noch eine Frage der zeit zu sein (wenn nicht was riesig schief geht)

https://investorrelations.sarepta.com/news-releases/news-rel…
Antwort auf Beitrag Nr.: 62.219.465 von paul81 am 23.12.19 10:33:27Sarepta Therapeutics erhält von Roche 1,15 Milliarden Dollar in bar im Austausch für die internationalen Rechte an der Gentherapie SRP-9001 für Duchenne-Muskeldystrophie.
Im Rahmen der Vereinbarung erhält Roche die kommerziellen Rechte an der Duchenne-Gentherapie SRP-9001 gegen 750 Millionen Dollar in bar und 400 Millionen Dollar in Sarepta-Aktien, die zu einem Preis von 158,59 Dollar pro Aktie erworben werden.
Sarepta hat außerdem Anspruch auf weitere Zahlungen in Höhe von 1,7 Milliarden US-Dollar, die an zukünftige regulatorische und wirtschaftliche Meilensteine gebunden sind. Wird die Gentherapie ausserhalb der USA zugelassen, zahlt Roche an Sarepta "mid-teens" Lizenzgebühren auf die Verkäufe. Die beiden Unternehmen teilen sich auch alle weltweiten Entwicklungskosten zu gleichen Teilen. Sarepta behält alle Rechte an SRP-9001 in den USA.
Duchenne wird durch eine vererbte Mutation in einem Gen verursacht, das Dystrophin produziert, ein Protein, das notwendig ist, damit die Muskeln richtig funktionieren. Die Krankheit betrifft fast immer Jungen. Ohne Dystrophin bauen die Muskeln mit der Zeit ab, und deshalb verlieren Duchenne-Patienten allmählich ihre Fähigkeit zu gehen und zu atmen. Die Krankheit ist tödlich, oft schon in den späten Teenagerjahren oder Anfang 20.
Sarepta's SRP-9001 ist eine einmalige, krankheitsmodifizierende Gentherapie, die für die große Mehrheit der Duchenne-Patienten geeignet ist. Zwei andere Medikamentenhersteller, Solid Biosciences (SLDB) und Pfizer (PFE), arbeiten an ähnlichen Gentherapien.
Im Rahmen der Vereinbarung erhält Roche die kommerziellen Rechte an der Duchenne-Gentherapie SRP-9001 gegen 750 Millionen Dollar in bar und 400 Millionen Dollar in Sarepta-Aktien, die zu einem Preis von 158,59 Dollar pro Aktie erworben werden.
Sarepta hat außerdem Anspruch auf weitere Zahlungen in Höhe von 1,7 Milliarden US-Dollar, die an zukünftige regulatorische und wirtschaftliche Meilensteine gebunden sind. Wird die Gentherapie ausserhalb der USA zugelassen, zahlt Roche an Sarepta "mid-teens" Lizenzgebühren auf die Verkäufe. Die beiden Unternehmen teilen sich auch alle weltweiten Entwicklungskosten zu gleichen Teilen. Sarepta behält alle Rechte an SRP-9001 in den USA.
Duchenne wird durch eine vererbte Mutation in einem Gen verursacht, das Dystrophin produziert, ein Protein, das notwendig ist, damit die Muskeln richtig funktionieren. Die Krankheit betrifft fast immer Jungen. Ohne Dystrophin bauen die Muskeln mit der Zeit ab, und deshalb verlieren Duchenne-Patienten allmählich ihre Fähigkeit zu gehen und zu atmen. Die Krankheit ist tödlich, oft schon in den späten Teenagerjahren oder Anfang 20.
Sarepta's SRP-9001 ist eine einmalige, krankheitsmodifizierende Gentherapie, die für die große Mehrheit der Duchenne-Patienten geeignet ist. Zwei andere Medikamentenhersteller, Solid Biosciences (SLDB) und Pfizer (PFE), arbeiten an ähnlichen Gentherapien.
Antwort auf Beitrag Nr.: 62.221.145 von Cyberhexe am 23.12.19 14:36:02
Ausgangsfrage: Totalverlust oder Tenbagger?
Das wird wohl mehr wie ein Verzehnfacher!!
Zitat von Cyberhexe: Sarepta Therapeutics erhält von Roche 1,15 Milliarden Dollar in bar im Austausch für die internationalen Rechte an der Gentherapie SRP-9001 für Duchenne-Muskeldystrophie.
Im Rahmen der Vereinbarung erhält Roche die kommerziellen Rechte an der Duchenne-Gentherapie SRP-9001 gegen 750 Millionen Dollar in bar und 400 Millionen Dollar in Sarepta-Aktien, die zu einem Preis von 158,59 Dollar pro Aktie erworben werden.
Sarepta hat außerdem Anspruch auf weitere Zahlungen in Höhe von 1,7 Milliarden US-Dollar, die an zukünftige regulatorische und wirtschaftliche Meilensteine gebunden sind. Wird die Gentherapie ausserhalb der USA zugelassen, zahlt Roche an Sarepta "mid-teens" Lizenzgebühren auf die Verkäufe. Die beiden Unternehmen teilen sich auch alle weltweiten Entwicklungskosten zu gleichen Teilen. Sarepta behält alle Rechte an SRP-9001 in den USA.
Duchenne wird durch eine vererbte Mutation in einem Gen verursacht, das Dystrophin produziert, ein Protein, das notwendig ist, damit die Muskeln richtig funktionieren. Die Krankheit betrifft fast immer Jungen. Ohne Dystrophin bauen die Muskeln mit der Zeit ab, und deshalb verlieren Duchenne-Patienten allmählich ihre Fähigkeit zu gehen und zu atmen. Die Krankheit ist tödlich, oft schon in den späten Teenagerjahren oder Anfang 20.
Sarepta's SRP-9001 ist eine einmalige, krankheitsmodifizierende Gentherapie, die für die große Mehrheit der Duchenne-Patienten geeignet ist. Zwei andere Medikamentenhersteller, Solid Biosciences (SLDB) und Pfizer (PFE), arbeiten an ähnlichen Gentherapien.
Ausgangsfrage: Totalverlust oder Tenbagger?
Das wird wohl mehr wie ein Verzehnfacher!!
Kursreaktion aber sehr verhalten bei DEM Deal...🤔
Antwort auf Beitrag Nr.: 62.221.829 von Stoxtrayder am 23.12.19 16:15:20Morgen gibts Ergebnisse:
https://investorrelations.sarepta.com/news-releases/news-rel…
https://investorrelations.sarepta.com/news-releases/news-rel…
Guten Abend,
darf ich einmal fragen, wie ihr Sarepta derzeit seht - nach dem Roche-Deal? Was sind die nächsten Schritte?
Die Aktie ist ja auch stark zurück gekommen, das darf man wohl auch Corona zuschreiben.
Danke für ein kurzes Update!
Gruß greenhorn
darf ich einmal fragen, wie ihr Sarepta derzeit seht - nach dem Roche-Deal? Was sind die nächsten Schritte?
Die Aktie ist ja auch stark zurück gekommen, das darf man wohl auch Corona zuschreiben.
Danke für ein kurzes Update!
Gruß greenhorn
Antwort auf Beitrag Nr.: 63.106.804 von greenhorn1998 am 23.03.20 20:59:08Sarepta is a name in biotech that’s also favored by the analysts at RBC Capital Markets in a recent note that looks ahead at 2021.
Analyst Brian Abrahams sees at least 8% upside for Sarepta’s $178 stock, if the first quarter of next year provides a good readout from the company’s first randomized, controlled trial of its gene therapy for Duchenne muscular dystrophy
https://www.barrons.com/articles/4-biopharma-stock-picks-fro…
Analyst Brian Abrahams sees at least 8% upside for Sarepta’s $178 stock, if the first quarter of next year provides a good readout from the company’s first randomized, controlled trial of its gene therapy for Duchenne muscular dystrophy
https://www.barrons.com/articles/4-biopharma-stock-picks-fro…
Absturz nach enttäuschenden DMD Daten.
https://www.globenewswire.com/news-release/2021/01/07/215523…
Ging ca. 50% runter. Scheint mir viel zu sein. Vielleicht eine Möglichkeit, auf eine kurzfristige Gegenbewegung zu spekulieren. Was meint ihr?
https://www.globenewswire.com/news-release/2021/01/07/215523…
Ging ca. 50% runter. Scheint mir viel zu sein. Vielleicht eine Möglichkeit, auf eine kurzfristige Gegenbewegung zu spekulieren. Was meint ihr?
https://www.greenleiter.com/post/antisense-shares-are-on-fir…
schlechte Nachrichten für Sarepta auf DMD. aber gute Nachrichten für Antisense ....
schlechte Nachrichten für Sarepta auf DMD. aber gute Nachrichten für Antisense ....
Significant global biotech interest moving to therapeutic treatment now of DMD
https://www.greenleiter.com/post/antisense-shares-have-incre…
https://www.greenleiter.com/post/antisense-shares-have-incre…
https://www.nextbiotech.com.au/anp-rapidly-advance-phase-iib…
Sarepta's former chairman is now a non-executive director of Antisense...wonder if they will do a deal for DMD
Sarepta's former chairman is now a non-executive director of Antisense...wonder if they will do a deal for DMD
https://www.sharecafe.com.au/2021/01/14/antisense-therapeuti…
things dont look good for Sarepta .....
things dont look good for Sarepta .....
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -3,14 | |
| -0,78 | |
| -0,11 | |
| -0,70 | |
| -2,34 | |
| -0,15 | |
| -3,40 | |
| -1,46 | |
| -0,69 | |
| -3,26 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 167 | ||
| 104 | ||
| 79 | ||
| 66 | ||
| 50 | ||
| 49 | ||
| 36 | ||
| 29 | ||
| 28 | ||
| 22 |





















